当社は、国立研究開発法人産業技術総合研究所(創薬分子プロファイリング研究センター・機能プロテオミクスチーム・五島直樹研究チーム長)が構築したリソースや開発した技術を移転し、これらを基に高精度の免疫プロファイリングを実現し、診断・創薬・再生医療の分野に革新的な研究デザインを提供します。
3つの独自リソース・技術(産総研から独占的ラインセンスを取得)
1.ヒトcDNAクローンリソースHuPEX®の活用
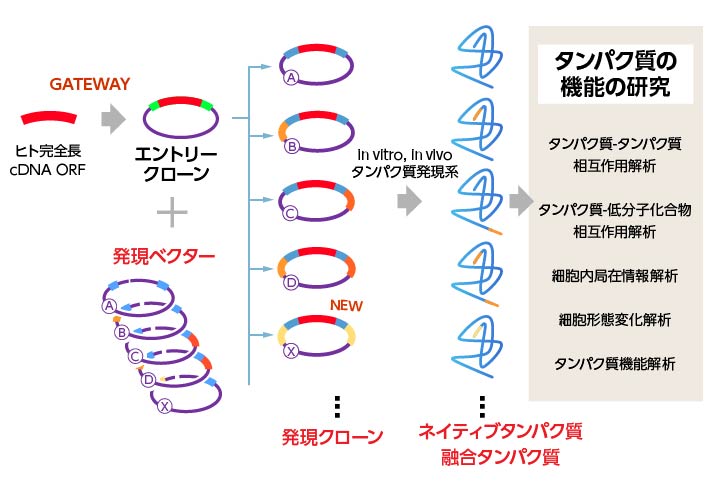
ヒト完全長cDNAクローンを基にしてGatewayシステムによってエントリークローンを作製し、ヒト・プロテオーム発現リソース(Human Proteome Expression Resource, HuPEX®)を構築しています。
現在までに、HuPEX®は1.4万種類のエントリークローンが整備されており、既知のヒト遺伝子の3/4以上をカバーしており、世界最大級のヒト・タンパク質を発現するための汎用的リソースとなっています。HuPEX®を使用することで、目的タンパク質を様々なタンパク質発現系で発現するための発現クローン作製を容易にします。また、タンパク質機能解析のためには多種類のタンパク質をN末端やC末端に様々なタグを付加して発現することが必要になります。HuPEX®は多種類のタンパク質を発現するための発現クローンをハイスループットに作製することが可能です。
網羅的ヒト・タンパク質機能解析のための基盤構築
ヒト完全長cDNA ⇒ HuPEX® ⇒ 様々な発現クローン
2.プロテオームワイドなタンパク質合成技術
タンパク質発現系は、他の発現系に比べ発現効率・可溶化率に優れているコムギ胚芽無細胞系を採用しています。
この技術は、96-384ウェルプレート上で、エントリークローンから鋳型DNA構築、RNA合成、タンパク質合成までのすべての工程を反応物と試薬の分注操作のみで実現させることが出来ます。そのため、1000種類のエントリークローンから、最短1週間でタンパク質合成までおこなうことが可能です。
コムギ無細胞系によるプロテオームワイドなタンパク質合成

この技術で1.4万種類のヒト・タンパク質を合成した結果、95%以上でタンパク質発現の確認ができました。
複数タンパク質の共発現
この技術は複数の鋳型DNA(PCR産物)を混合して、1チューブ内でRNA合成→タンパク質合成することで、タンパク質を共発現することも可能です。 これまでに約1000種類のタンパク質の共発現をおこない、定量MS解析で個々のタンパク質の発現が確認できています。
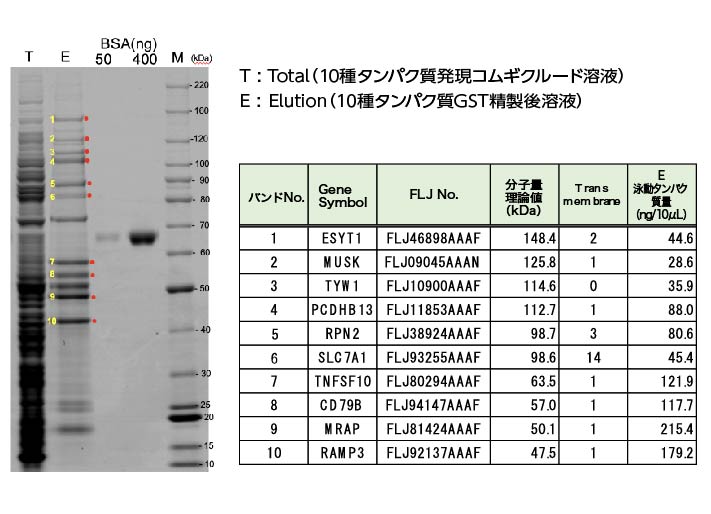
コムギ無細胞系による10種タンパク質の共発現
N末端FLAG+GSTタグ付き発現クローン10種類
10種DNA鋳型混合⇒RNA合成⇒タンパク質合成⇒GST精製⇒SDS-PAGE⇒CBB染色
3.タンパク質アレイ作製技術
当社のタンパク質アレイは、HuPEX®からコムギ胚芽無細胞系によりプロテオームワイドに合成したタンパク質を、高密度でアレイ基板に非乾燥状態で搭載しています。
アレイ搭載のタンパク質
N末端側にGST+FLAGタグを付加したかたちで、コムギ胚芽無細胞系により発現させたタンパク質をクルード溶液の状態(精製しない)で、グルタチオン(GSH)を表面修飾したアレイ基板にスポットし、非乾燥状態でアレイ基板に結合(GST-GSH特異的結合)させます。アレイの作製後、搭載したタンパク質が変性しないようにアレイを保存溶液に浸漬し、冷凍保存します。その後、使用するときにアレイ(タンパク質)を解凍し、測定に使用します。すなわち、アレイ作製から測定までの全ての工程において、アレイに搭載されたタンパク質は「ウェット」な状態で保たれています。
アレイ搭載タンパク質のスポット方法
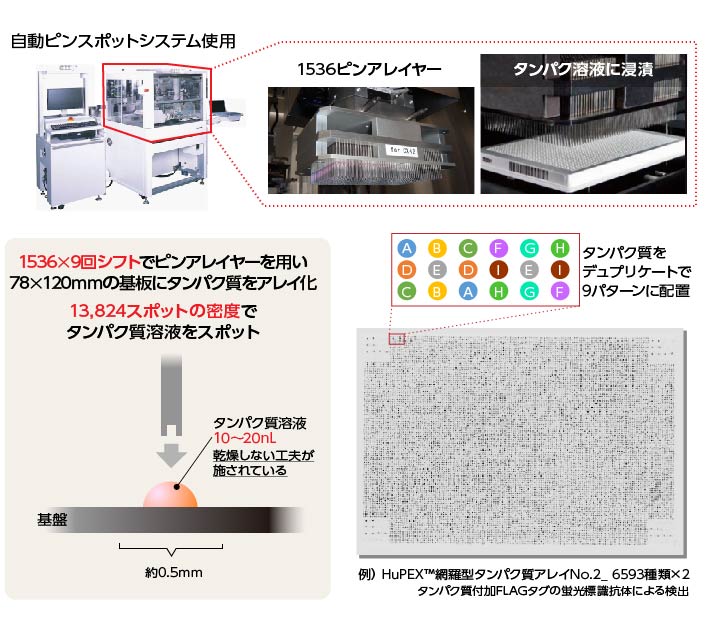
78×120mmのアレイ基板に、分注チップを使用して384 または 1536個の液滴をスポットする方法(フォーカス型アレイやカスタムアレイ用)と1536本のピンツールを使用して13,824個の液滴をスポットする方法(網羅型アレイ用)の2種類があります。
1536ピンツールを使用してスポットする場合、液滴の容量は10-20nLと超微量ですが、タンパク質が乾燥しない工夫を施しております。フォーカス型アレイ、カスタムアレイおよび網羅型アレイは、アレイ方法の違いによる搭載タンパク質の状態の違いはありません。
384 または 1536タンパク質スポットアレイ_チップ方式

13,824タンパク質スポット高密度アレイ_ピンツール方式
HuPEX®タンパク質アレイの性能
自己免疫プロファイリングの実施例
HuPEX®クローンから合成されたタンパク質をすべて搭載した網羅型タンパク質アレイ(No.1-3の3枚)を使用して、傍腫瘍性小脳変性症患者血清に含まれている自己抗体を検出しました。
傍腫瘍性小脳変性症患者血清からの自己抗体検出

検出できた抗体の中には、複数のがん抗原に対する抗体や既知の自己免疫疾患のマーカー抗体がありました。その中で疾患特異的な傍腫瘍性神経症候群の自己抗体マーカーである抗Ri抗体(抗原はNOVA1)も含まれていました。
これは、この患者さんの臨床診断が、悪性腫瘍を伴って自己免疫学的機序により生じる、小脳性運動失調を呈する神経疾患であることから、矛盾のない結果でした。
